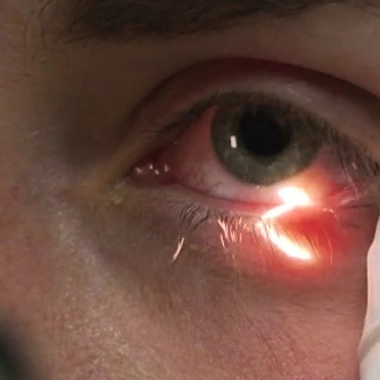
Patch contre l'allergie à l'arachide : quel taux de réponse au traitement ?
Suite à la parution le 6 mars 2017, à 12h45, de notre article intitulé "Patch contre l'allergie à l'arachide : une annonce trompeuse", la société en charge de la communication de DBV technologies, ainsi que l'entreprise elle-même, ont tenu à nous apporter quelques précisions.
Rédigé le , mis à jour le

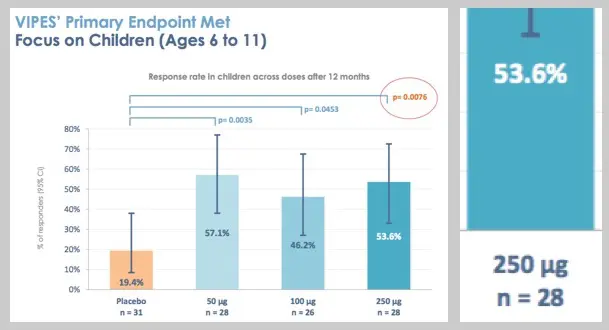
Extrait d'une documentation transmise par DBV technologies, datée de février 2017, précisant que 28 enfants se sont vu proposer le traitement Viaskin® Peanut 250 μg durant l'année où s'est déroulée l'essai VIPES.
Communication et pourcentages
Suite à la parution de notre article intitulé "Patch contre l'allergie à l'arachide : une annonce trompeuse", la société en charge de la communication de DBV technologies a tenu à nous communiquer des informations complémentaire par message électronique : "L'étude OLFUS-VIPES compte bien au total 171 patients : 97 enfants, [et] 74 adolescents et adultes. Parmi les 97 enfants, DBV Technologies a étudié la tranche d'âge 6-11 ans, soit 18 enfants – et donc les 83,3% représentent 15 enfants." Ils précisent ces résultats "excellents", qui concernent l’enfant, "viennent conforter ceux qui ont eu lieu sur les autres tranches d’âge".
Nous leur rappelons que notre article mettait en question l’affirmation qu’eux-mêmes nous avaient communiqués plus tôt dans la matinée, selon laquelle le 83,3% se rapportait à 171 patients… ainsi que le procédé contestable qui consiste à tirer un pourcentage de 18 cas. Aucune donnée ne nous ayant été communiquée concernant les taux d’efficacité sur l’adulte et l’enfant (y compris à l’heure où nous publions cette mise à jour), nous avons cherché à établir le taux sur la base de leurs propres informations.
Alors, quel est le taux d’efficacité du fameux patch ?
Des informations plus précises sur l’essai clinique nous ont finalement été communiquées dans l’après-midi par David Schilansky, directeur général délégué de DBV Technologies. Selon lui le communiqué de presse s’est voulu "plus simple que celui d’octobre 2015", à destination "de journalistes qui ne cherchent pas forcément à rentrer dans les détails des chiffres".
Voici ses explications. Une première étude, baptisée VIPES, et destinée à identifier la dose optimale du traitement, a été menée sur 221 patients, parmi lesquels 28 enfants sous patchs dosés à 250 μg (voir illustration ci-contre). Cette étude a duré un an, et a conclu à l’intérêt de ce dosage (53,6% de réponse au traitement après 12 mois). Une seconde étude, OLFUS-VIPES, a visé à suivre des patients, uniquement traités patchs dosés à 250 μg : elle a impliqué 171 participants de VIPES, "dont 18 enfants (6-11 ans) qui avaient [tous utilisé] un patch dosés à 250 μg" durant la première étude. Aussi juge-t-il tout à fait honnête le fait que le communiqué de presse diffusé ce 5 mars annonce qu’"il a été montré que 83,3 % des enfants ont répondu à Viaskin® Peanut 250 μg au bout de trois ans de traitement, sans qu’aucun évènement indésirable grave lié au traitement ne soit observé." David Schilansky précise qu’il faut considérer qu’OLFUS-VIPES est une étude "différente de VIPES".
Les informations relatives aux autres tranches d’âge "sont présentées dans les abstracts [1] mais ne font pas l’objet d’une communication", note le directeur général délégué. Il confirme que ces données-ci ne sont "pas toutes [statistiquement] significatives" et qu’aujourd’hui, la cible du traitement est "clairement, les enfants" – d’où l’objet, très spécifique, du communiqué.
15 enfants sur 18… ou sur 21 ? ou sur 28 ?
En dépit de ces explications, les termes du communiqué nous posent toujours problème. Tout d'abord, constatons que les documents transmis par DBV technologies précisent qu'au début d'OLFUS-VIPES non pas 18, mais 21 enfants étaient inclus (voir ci-dessous).

Extrait d'une documentation transmise par DBV technologies, datée de février 2017, précisant que 21 étaient initalement inclus dans l'essai OLFUS-VIPES.
Il est possible de dire que 15 des 18 enfants participants à OLFUS-VIPES, qui avaient déjà bénéficié d’une année de traitement (parmi 28 enfants), et suivis sur deux ans supplémentaires, ont répondu au traitement. Extrapolée à la population générale, le taux de réponse pourrait être beaucoup plus faible que 83,3%, compte tenu des marges d’erreur associées à un si faible échantillon. Soulignons encore que, même voisin de 50% ou 60%, cette stratégie de désensibilisation resterait très intéressante, compte tenu des enjeux sanitaires associés à l’allergie.
Mais l’affirmation selon laquelle "il a été montré que 83,3 % des enfants ont répondu à Viaskin® Peanut 250 μg au bout de trois ans de traitement […]" reste douteuse. Le nombre d’enfants mis sous Viaskin® Peanut 250 μg trois ans avant la présentation des résultats était de 28. Le nombre de patients chez qui la réponse au traitement a pu être évaluée est certes de 18… mais si l’on cherche à identifier le taux de réponse positive sur trois ans, il faut le réaliser sur l’échantillon inclus trois ans plus tôt (soit 15 enfants sur 28, ou "53,6%" si l’on commet une mise en pourcentage). Considérant qu'OLFUS-VIPES est "une étude différente de VIPES", l’annonce aurait dû parler d’un taux de réponse de 15/18 à deux ans, chez des enfants qui n’ont pas abandonné le traitement au bout d’un an. Ce qui est quelque peu différent de l’annonce initialement diffusée.
Notre article n’avait – et n’a toujours – absolument pas vocation à discréditer un traitement potentiellement prometteur, mais bien à mettre en évidence la difficulté à accéder à une information capitale (absente des dépêches de presse) : le nombre de patients auquel se rapporte l’enthousiasmant "taux de réponse" largement diffusé.
[1] Les résumés des études ou des annonces en congrès, NDLR.